4.4.3 Unbestimmtheitsprinzip in 3D
4.4.2a Beispiel: Unschärferelation beim Wasserstoffatom
Radius: nm
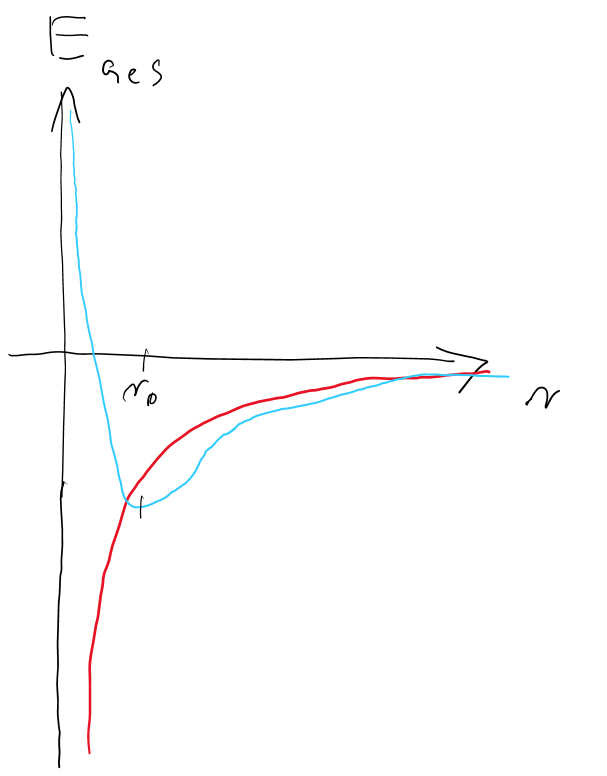
Beispiel: Energie des Elektrons
klassisch Energie (falsch!)
Zentripetalbeschleunigung
klassisch: würde in den Kern stürzen
QM: Unschärferelation
, da und , da
Annahme
aus
Bohrsche Radius
m
eV
Annahme war gut gewählt.
Achtung: Streng genommen gilt Unschärferelation nur für die gleiche Komponenten , hier vergleicht man Tangentialimpuls mit Radius.
Wir werden sehen, dass das Elektron in der Regel nicht auf einer Kreisbahn läuft sondern in Orbitale.
4.4.4 Unbestimmtheitsprinzip für Energie und Zeit
Oben:
analog:
Annahme:
Das heißt, existiert Zustand/ Teilchen nur kurz Energie unscharf Natürliche Linienverbreiterung von Spektrallinien
Beispiel: Wasserstoff

Übergang mit nm . Gesucht:
aber
4.6 Bohrsches Atommodell
Niels Bohr 1922 Nobelpreis
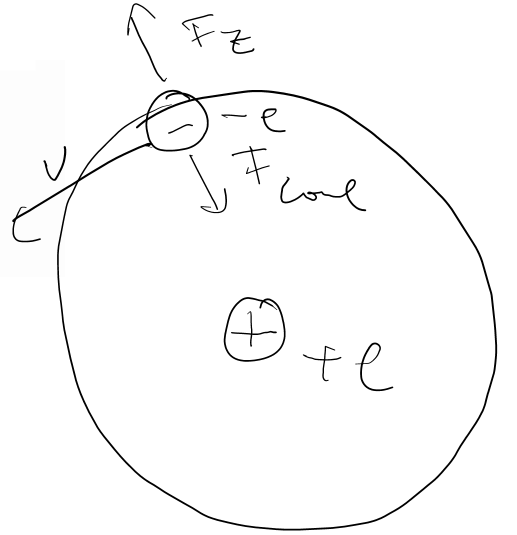
1)
Energie (eigentlich falsch):
Bohrsche Postulat:
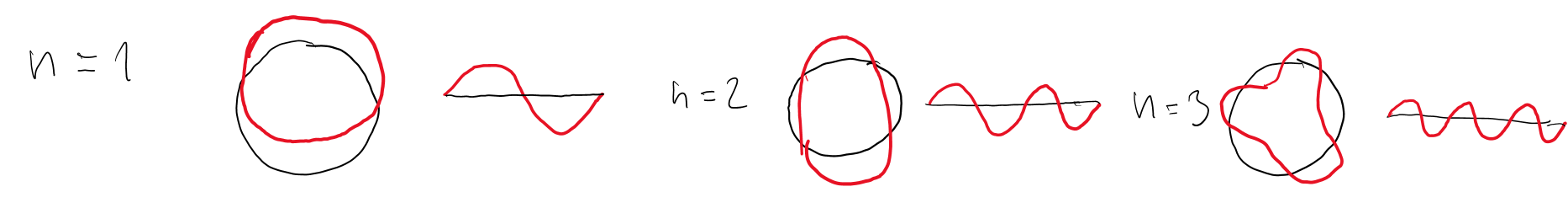
Wellenfunktion muss konstruktiv interferieren.Umfang: ,
De Broglie:
2)
1) in 2)
mit Bohrradius
in einsetzen
mit n=1,2,3,... und Z, der Kernladungszahl (für Wasserstoff: Z=1)